精准抗癌新标杆:抗体药物偶联物(ADCs)技术与Cytiva赋能方案
2025/08/28
在肿瘤治疗领域,传统化疗的“无差别杀伤”常导致严重副作用,而抗体药物偶联物(Antibody-Drug Conjugates, ADCs)凭借“精准靶向 + 强效杀伤”的双重优势,成为当前最具潜力的治疗手段之一。作为融合单克隆抗体选择性与细胞毒性药物的“生物导弹”,ADCs能精准定位肿瘤细胞、可控释放杀伤载荷,显著提升治疗指数。 ADCs:重构肿瘤治疗的“精准导弹”
ADCs 是由单克隆抗体(mAb)、细胞毒性药物(payload)、连接子(linker)组成的靶向免疫偶联物,通过“四步作用机制”实现肿瘤清除: 靶向结合:抗体与肿瘤细胞表面过表达抗原特异性结合; 内吞入胞:ADC-抗原复合物经受体介导内吞进入细胞; Payload释放:linker在溶酶体酸性环境或酶作用下断裂,释放payload; 肿瘤杀伤:payload干扰肿瘤细胞关键进程(如微管聚合、DNA修复),诱导凋亡,部分payload 还能通过“旁观者效应”清除邻近抗原阴性肿瘤细胞,克服异质性难题。 图1 ADCs的结构及作用机制 ADCs的核心优势在于:兼顾抗体的高选择性(减少健康细胞损伤)与payload的强效性(提升肿瘤杀伤率),同时允许更高剂量payload给药,突破传统化疗局限。 ADC核心组件的技术突破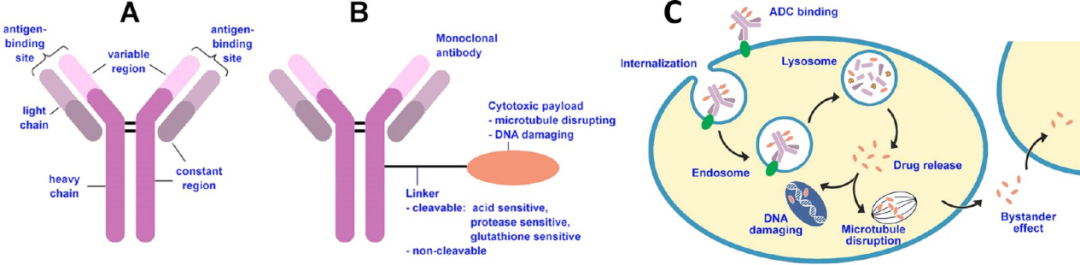
ADCs的性能依赖三大组件的协同优化,近年来各组件已实现从“非特异性”到“精准可控” 的升级: 01单克隆抗体:靶向导航的“精准定位器” 抗体是ADC的“导航核心”,需满足高特异性、低免疫原性、高效内化要求: 类型迭代:早期鼠源抗体易引发免疫反应,现主流为人源化IgG1,半衰期约21天;IgG4通过铰链区突变阻断Fab臂交换,用于特定靶点(如CD33、CD22); 新型设计:双表位抗体(如靶向HER2双结构域)增强结合亲和力,纳米抗体(约15 kDa)提升实体瘤穿透性,Probody技术通过肿瘤微环境蛋白酶激活抗体,降低脱靶毒性。 02Linker:Payload释放的“智能开关” Linker需平衡循环稳定性与胞内可切割性,分为两类: 可切割linker:占获批ADC主流(13款中11款采用),如酸敏感腙键、酶可切割Val-Cit二肽(Adcetris)、谷胱甘肽敏感二硫键,通过肿瘤微环境特性实现精准释放; 不可切割linker(如Kadcyla的MCC linker):依赖抗体溶酶体降解释放payload,避免payload 扩散至健康组织,降低系统毒性。 此外,分支型linker(Fleximer平台)可提升DAR至10-15,增强实体瘤疗效。 图2 ADC连接子类型 03Payload:肿瘤杀伤“强效弹药” Payload需具备nM-pM级活性,主流类型包括: 微管抑制剂:如Auristatins、Maytansinoids,通过阻断细胞分裂杀伤肿瘤; DNA 损伤剂:如喜树碱类、PBD二聚体,通过破坏DNA结构诱导凋亡; 新型payload(STING激动剂、GRM调节剂)正拓展ADC功能至免疫调节领域。 Cytiva:ADC开发全流程的关键赋能者 ADCs已成为肿瘤治疗的核心方向,其技术突破依赖三大组件的持续优化。Cytiva凭借其全方位、一站式的生物工艺解决方案,强力赋能ADC药物的高效开发与生产。从上游的高效细胞株构建和大规模抗体生产(Xcellerex生物反应器与HyClone培养基),到下游的精密层析纯化(ÄKTA系统与MabSelect填料)和关键质量属性分析(Biacore分子互作分析以确保结合活性),Cytiva的产品线确保了ADC核心抗体组分的高质量、高产量与高一致性,是您打造下一代“生物导弹”值得信赖的合作伙伴。 参考文献: Sasso J M, Tenchov R, Bird R, et al. The Evolving Landscape of Antibody−Drug Conjugates: In Depth Analysis of Recent Research Progress [J]. Bioconjugate Chemistry, 2023, 34 (10): 1951-2000.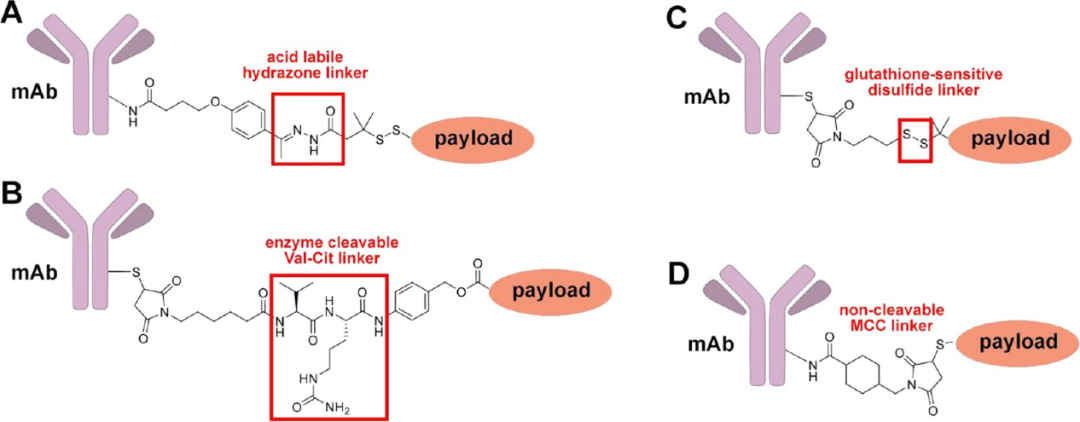
# END # 部分图片、字体、文字来源于网络 如有侵权请联系删除