分子克隆系列之传统克隆(酶切-连接克隆)—从粘性末端到 Golden Gate
2026/01/28

为什么传统克隆仍是实验室的 “压舱石”?
在 Gibson 组装、Gateway 克隆等 “高大上” 技术层出不穷的今天,传统酶切-连接克隆依然是全球超过 60% 基础实验室的shouxuan方案。它就像实验室里的 “压舱石”—— 技术成熟、成本可控、结果稳定,不仅是新手入门的第一课,更是复杂克隆项目的基础环节。
从最早的粘性末端克隆到如今 Type IIS 酶介导的 Golden Gate 模块化组装,传统克隆早已不是 “过时技术”,而是在不断进化中成为支撑合成生物学升级的底层工具。
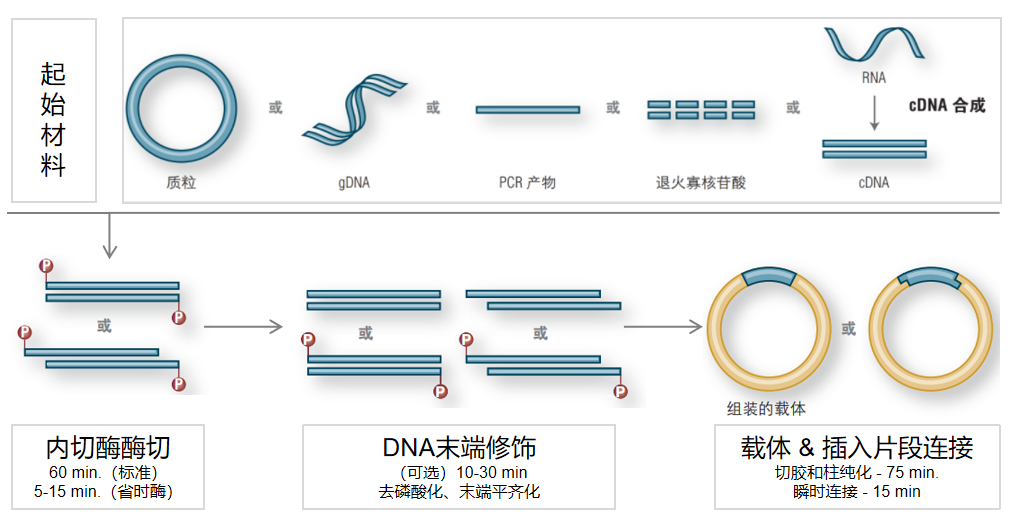
传统克隆技术流程图
一、粘性末端克隆
原理
传统的分子克隆利用限制性内切酶切割产生粘性末端以进行目标分子和载体的特异性连接[1]。然而,这种方法具有很大的局限性:当目标片段含有质粒多克隆位点上所有的限制性内切酶时,无论选哪一种限制性内切酶都将导致目标DNA片段的切割;在进行多个基因克隆时,因各基因序列不同引起的限制性内切酶的选择不一,使得多个基因的克隆变成一个浩大的工程[2]。
粘性末端克隆原理如下:限制性内切酶会在识别序列处特异性切割 DNA,产生互补的单链粘性末端(如 EcoRⅠ 切割后产生 5’-AATT-3’突出端)。当目的片段与载体被相同酶切后,两者的粘性末端可通过碱基互补配对结合,再由 T4 DNA 连接酶催化磷酸二酯键形成,最终构建重组载体。
1. 同酶切割:载体与外源DNA产生相同粘性末端,连接过程中会产生目的基因的正反向插入、载体或目的基因片段的自身环化、载体与单个或多个目的基因片段之间重组等几种不同结果,其中载体的自身环化最为常见,需调整目的基因相对载体的比例或用碱性磷酸酶(CIP)处理载体(脱磷酸),以阻止线性载体DNA分子自身环化
2. 异酶切割:载体与外源DNA由于不同种酶的黏性末端不匹配,避免了自身连接,外源DNA片段只能定向地连接到载体的两个酶切位点之间,阳性率更高。当然也会小概率的发生载体位点黏性末端之间两个碱基互补形成开环的情况,这样的重组子占少数。
适用场景
a. 常规短片段(<5kb)定向克隆,如质粒改造、启动子替换等基础载体构建。
b. 对成本敏感的实验室,试剂价格仅为无缝克隆试剂盒的 1/5~1/3
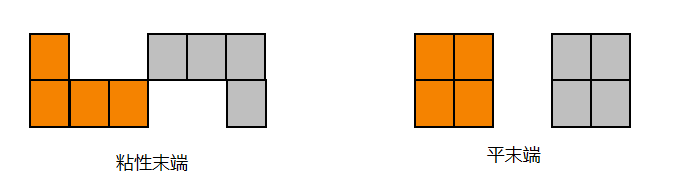
二、平末端克隆
原理
当 DNA 被平末端酶(如 EcoR V、HpaⅠ)切割,或 PCR 产物经高保真酶扩增后,会产生无突出端的平末端。T4 DNA 连接酶可催化平末端之间的连接,但效率仅为粘性末端的 1/10~1/5,依赖更高酶量与更长反应时间提升效率。
适用场景
a. 无合适粘性末端的片段拼接,如 PCR 产物为平末端、目的基因内部含所有可用粘性酶切位点。
b. 简单片段的融合克隆,如标签蛋白与目的基因的 C 端融合。
备注:(末端修饰替代)若 PCR 产物为平末端,可先用 Taq 酶在 72℃延伸 10min,在 3’端加 A 后转为 TA 克隆,效率更高。
总结:
需要限制性内切酶和连接酶的克隆方法——平末端克隆和粘性末端克隆。
这是最为传统、最为经典的基因克隆方法,也是目前仍然被广泛使用的克隆方法,特别是粘性末端克隆法,它需要限制性内切酶和连接酶的参与,而且受限制性内切酶酶切位点的限制和连接酶效率的影响。平末端克隆操作简便,但是克隆效率却很低,而且克隆非定向性,即会出现基因的反向插入和正向插入两种可能。粘性末端克隆需要在目的片段 5' 末端引入相对应的酶切位点,而且酶切效率会影响克隆效率。粘性末端克隆具有定向性,但是对于长片段来说,其克隆效率也是比较低的,甚至片段越长,克隆效率越低。
三、TA 克隆
原理
TA 克隆无需限制性内切酶,仅依赖连接酶即可完成克隆:Taq DNA 聚合酶扩增 PCR 产物时,会在 3’端非特异性添加一个 A 碱基;TA 克隆载体 3’端预先添加 T 碱基,通过 A-T 碱基配对快速连接,直接实现 PCR 产物克隆,无需设计酶切位点。
技术升级:
改进型 TA 克隆(如 TOPO-TA)将 T 载体改为平末端载体,结合拓扑异构酶 Ⅰ 的作用,可直接插入平末端 PCR 产物(如 Pfu DNA 聚合酶扩增的 PCR 产物),无需加 A 尾处理,兼顾平末端克隆的便捷性与 TA 克隆的高效率
适用场景
a. PCR 产物的快速克隆与验证,如 cDNA 克隆、基因突变体构建。
b. 未知序列片段的克隆,无需提前分析酶切位点。
c. 高通量克隆场景,如 cDNA 文库构建。
四、Type IIS 酶介导克隆(Golden Gate/MoClo)
原理
Golden Gate 克隆有时被称为 MoClo,核心是酶切位点与切割位点分离。
该技术在形成入门克隆的时候引入一个 II 型限制性内切酶的酶切位点,这个酶切位点正好在重组酶特异性识别位点与外源 DNA 序列之间(切割位点位于识别序列外侧 3-4bp)。通过在引物中加入酶切位点和 4bp 自定义粘性末端,酶切后载体与片段会暴露互补的粘性末端,可实现多片段一步定向组装,且连接产物中无酶切位点残留,达到 “无缝无疤痕” 效果。
虽然说Golden Gate 技术是通过一步重组反应形成入门克隆,入门克隆与目标载体之间的目的基因的转载却是在限制性内切酶和连接酶的作用下完成的,所以这个技术还是一项需要限制性内切酶和连接酶的克隆方法。而且要求入门载体和目标载体具有同一限制性内切酶酶切位点,所以会增加选择限制性内切酶酶切位点的难度。 (可以借助NEB官网的Golden Gate在线设计工具https://goldengate.neb.com)
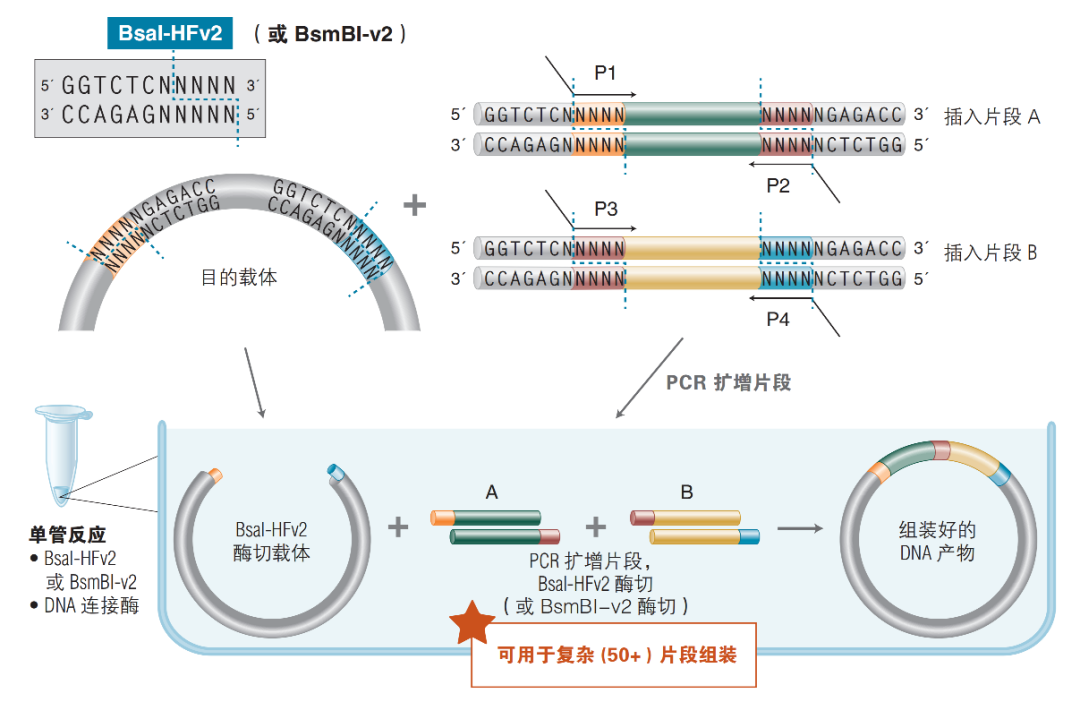
Golden Gate 组装原理图(来源:NEB官网)
适用场景
a. 合成生物学标准化模块组装,如 MoClo 体系用于代谢通路基因簇的快速搭建。
b. 多基因载体构建,如植物抗虫 - 抗除草剂双基因载体、哺乳动物细胞多荧光标记载体。
c. 大片段模块替换,如对现有载体的启动子、终止子进行精准替换。
优势
标准化降本:MoClo 体系将启动子、CDS、终止子等元件标准化为 “生物砖”,不同实验室可直接复用,降低重复构建成本。
多片段效率:NEB 的 Golden Gate Assembly Mix 可实现 12 个片段同步组装,阳性率超 95%,大幅缩短合成生物学项目周期。
传统克隆试剂的选型
常规实验优先国产试剂控成本,高难度、长片段 、精准构建选进口试剂,高通量 / 批量实验侧重国产性价比,长片段(>5kb)建议避开平末端 / TA 克隆,改用 Golden Gate 或无缝克隆。
对于粘性末端克隆:基础克隆shouxuan,对于限制性内切酶和T4连接酶的选择其实是有一些策略的,根据片段、成本、实验时长选择,要考虑载体自环需调片段比例或脱磷酸处理。
对于平末端克隆:连接效率比粘性末端的低,仅适配简单片段拼接,成本低但需多筛克隆,是无粘性末端时的备选。
对于TA 克隆:Taq 酶 PCR 产物快速克隆专用,根据产物片段大小及浓度高低、试剂成本选国产或进口。无 A 尾产物需先加 A,蓝白斑载体可减少验证工作量。
对于Golden Gate 组装:模块化多片段克隆专用,进口 NEB 试剂盒支持≤12 片段、高 GC 序列,阳性率≥95%,国产试剂盒支持≤8 片段、常规序列,成本减半,看片段数量和序列复杂度。
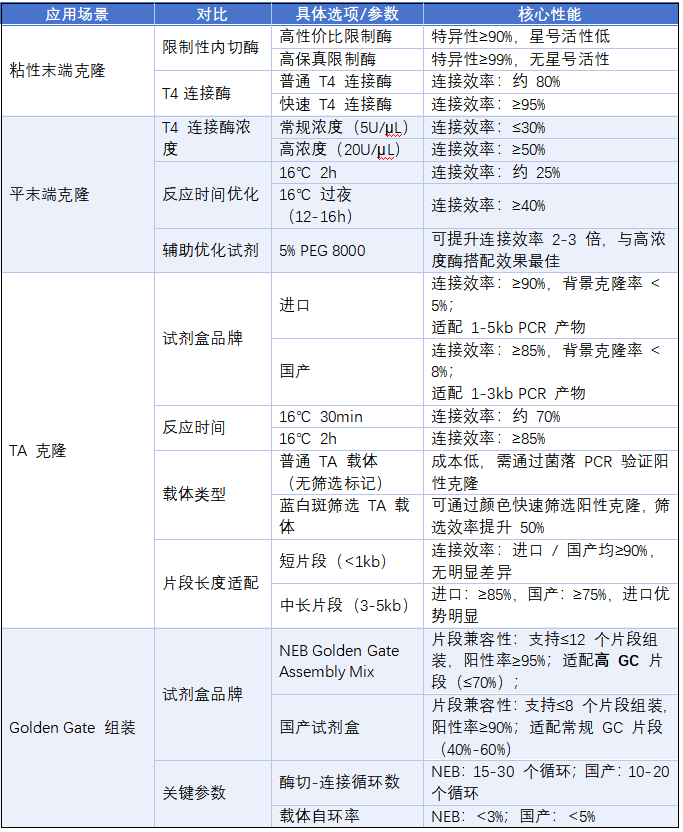
NEB产品推荐
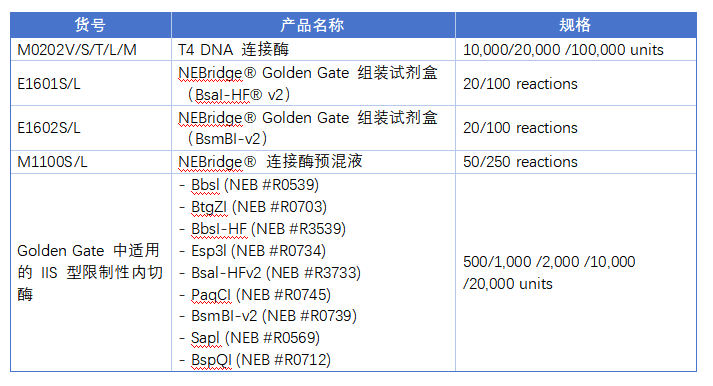
传统克隆从未因新技术的涌现而褪色: 粘性末端克隆的稳定可靠、TA 克隆的便捷高效、Golden Gate 的模块化创新,共同构成了基因操作的基础体系。它既是新手入门钥匙,帮助理解酶切、连接的核心逻辑;也是高手进阶武器,在合成生物学标准化构建中发挥不可替代的作用。
掌握传统克隆的避坑技巧(如粘性末端克隆的防自环策略),理解不同方法的适配场景,不仅能解决日常实验中的克隆难题,更能为后续学习无缝克隆、位点特异性重组克隆等进阶技术筑牢根基。下一篇,我们将解锁 “无酶切位点限制” 的无缝克隆技术,看看它如何通过同源重组实现多片段高效组装,敬请期待!
参考文献:
[1] Wilson R H, Morton S K, Deiderick H, et al. Engineered DNA ligases with improved activities in vitro[J ]. Protein Eng Des Sel, 2013,26:471- 478.
[2] Luft J R, Snell E H, Detitta G T. Lessons from high- throughput protein crystallization screening: 10 years of practical experience [J]. Expert Opin Drug Discov, 2011, 6:465- 480.
版权声明:本文为个人整理文章,内容仅供参考,旨在促进学术交流与信息共享,如有异议或侵权,请联系我们处理。
# END #
关于康成百澳生物
生命科学领域快速消费品及配套服务的专业供应商,总部位于泰州医药城,上海、广州、南京、成都、苏州、杭州、武汉等地设有分公司及办事处。
产品线涵盖精准医疗、抗体、疫苗、CGT、分子生物学与细胞生物学、常规临床检验、药物筛选、基因组学与蛋白质组学等研究和应用领域,以“技术+产品+服务”的一体化模式服务客户。

部分图片、字体、文字来源于网络 如有侵权请联系删除
