CGT行业新规落地:工艺与设备核心新要求
2026/02/27

2026年,CGT行业监管新规正式落地,彻底告别“重创新、轻合规”阶段,转向合规与质量双轮驱动。新规以“全链条可控、数据可靠、安全可及”为核心,对CAR-T、干细胞等产品的工艺、设备提出硬性要求。 新规核心导向:从“能生产”到“合规生产、稳定生产” 2026版CGT新规聚焦全生命周期管控,4大硬性导向缺一不可: 全流程封闭化:杜绝开放操作,无菌保障水平达10-6级; 工艺确定性:关键工艺参数(CPP)与关键质量属性(CQA)一一对应、可追溯; 数据完整性:遵循ALCOA+原则,生产数据实时自动采集、不可篡改; 规模化兼容:研发与商业化工艺无缝衔接,支持标准化量产。 工艺端新要求:全链条合规升级 工艺开发:建立“工艺-质量-临床”桥接证据链 新规要求工艺开发兼顾创新与合规,形成从实验室到商业化的完整桥接数据链,证明各阶段工艺一致性;CPP与CQA需明确对应并经多批次验证,完成3批可比性研究并获批。 工艺验证:升级为“全场景验证” 淘汰“三批合格即通过”模式,验证需覆盖临床、中试、商业化全阶段,模拟多场地、多批次一致性;多中心临床样品需单独验证,影响CQA的工艺变更需提前申报并提交完整佐证材料。 无菌与污染控制:全程封闭管控 强制淘汰开放式手工操作,细胞处理、培养等全流程采用封闭系统;洁净区分级调整,开放式操作提至B级,封闭式自动化工艺可降至D级,需配套在线无菌监测与报警系统。 数据完整性:ALCOA+落地执行 生产相关数据(参数、检测、日志等)需严格遵循ALCOA+原则,实时自动采集、禁止人工篡改;建立产品全生命周期追溯体系。 设备端新要求:自动化、封闭化、数字化成门槛 核心设备选型:封闭、一次性、模块化成标配 淘汰开放式、非标准化设备,核心设备需满足三大特点,规避交叉污染风险: 细胞分离/培养:全封闭一次性系统,自动化操作、减少人工干预; 生物反应器:转向一次性设备,支持细胞高密度、均一性培养; 转染/载体设备:适配密闭自动化工艺,支持规模化生产、具备在线监测; 制剂/灌装:无菌封闭系统,适配“小批量、多批次”生产特点。 设备性能:高精度、高稳定、高合规 关键参数(温度、pH等)实时闭环控制,波动范围严格把控;设备支持7×24小时连续运行,具备应急备份功能;与产品接触部件需符合生物相容性认证,可耐受灭菌。 数字化与自动化:配套合规采集系统 设备需自带数据采集系统(DCS),自动生成符合GMP的电子批记录;鼓励AI智能质控,设备软件需符合GAMP 5分类并完成IQ/OQ/PQ验证。 配套设施:同步升级 洁净区压差需达标,关键区域保持相对负压;公用介质(纯化水等)在线监测、符合专用标准;设备布局遵循“三流分离”,封闭设备可精简洁净区面积,配套CIP/SIP功能。 合规不踩坑,Cytiva与你同行 面对新规严苛要求,一套成熟合规的解决方案是企业抢占先机的关键。Cytiva打造覆盖“细胞分离-培养-扩增-纯化-制剂”全流程合规解决方案,Sepax C-Pro、Xuri™系列反应器、ÄKTA™纯化系统及Chronicle™数字化软件,精准匹配新规所有要求,助力企业加速产品研发与商业化落地。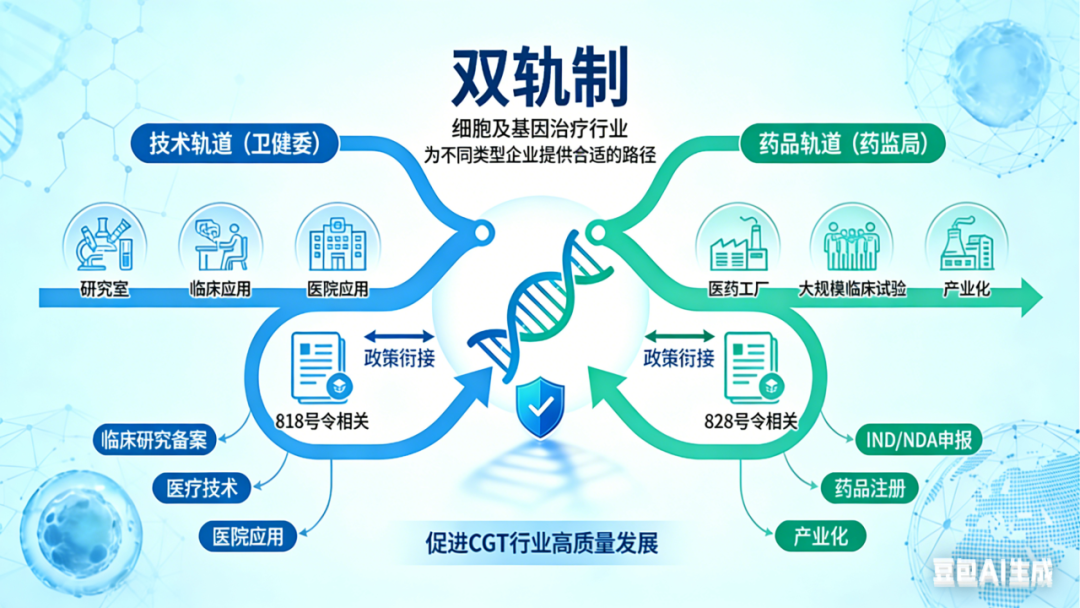

END 关于康成百澳生物 生命科学领域快速消费品及配套服务的专业供应商,总部位于泰州医药城,上海、广州、南京、成都、苏州、杭州、武汉等地设有分公司及办事处。 产品线涵盖精准医疗、抗体、疫苗、CGT、分子生物学与细胞生物学、常规临床检验、药物筛选、基因组学与蛋白质组学等研究和应用领域,以“技术+产品+服务”的一体化模式服务客户。 部分图片、字体、文字来源于网络 如有侵权请联系删除