技术干货 | 基于 GMP/ISO 标准的疏水性除菌滤器完整性检测流程与要点
2026/05/09

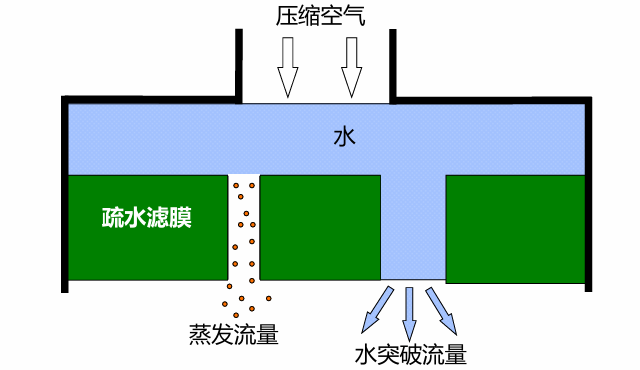
完整性检测 在制药、生物制品等行业,“无菌”是不可逾越的红线,疏水性除菌滤器是无菌保障的关键,其完整性验证是GMP及ISO相关标准(如ISO 13485)的硬性要求,直接关系产品合规性、患者安全,核心是证明滤器在使用全周期无破损、泄漏,能有效截留≥0.22μm微生物。 01、为什么完整性检测“非做不可”? 空气滤器应用:压缩空气系统、反应器进气和尾气过滤器、冻干机气体通道、环境空气过滤等应用广泛。 完整性验证不是“多此一举”,是合规和安全的双重要求。除菌滤器(如PTFE材质)完整性,直接对应其除菌效率(通常要求截留≥0.22μm的微生物),而验证的本质,是通过科学方法证明:滤器在生产放行、使用前后、存储安装、运输、灭菌等环节,未出现破损、堵塞、泄漏等异常,能持续满足无菌保障要求。 非破坏性完整性检测是对微生物拦截能力的间接反映。 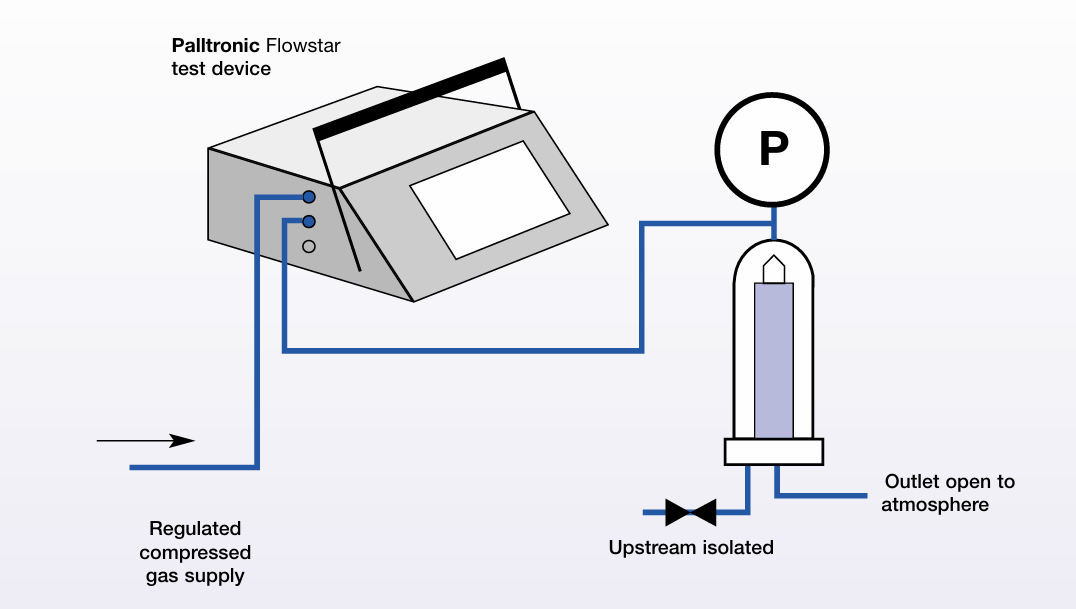
合规要求:GMP明确规定,除菌滤器在使用前必须进行完整性测试,使用后需进行回顾性验证(部分场景需即时验证);ISO标准则针对不同行业(如医疗器械、食品接触),要求验证过程可追溯、数据可核查,未按标准执行将直接影响产品上市、体系审核。
质量风险:滤器若存在微小破损,会导致微生物泄漏,进而引发产品污染、批次报废,甚至引发医疗安全事故,完整性验证是规避该风险的关键手段。
流程闭环:验证数据是滤器使用有效性的直接证据,需纳入企业质量档案,形成“选型-验证-使用-报废”的全流程追溯,满足审计要求。
何时该做完整性检测? 中国GMP 除菌过滤器使用后,必须采用适当的方法立即对其完整性进行检查并记录。常用的方法有起泡点试验、扩散流试验或压力保持试验。 美国cGMP 过滤器的完整性检测可以在使用前进行,并且应当在使用后常规进行。 欧盟GMP 除菌过滤器的完整性,需要使用适当的方法,在灭菌后,使用前进行确认,并需要在使用后立刻进行确认,包括气泡点、扩散流或压力保持测试。 02、疏水性滤器完整性测试方法 水侵入法(首推,疏水膜适用,操作简便) 疏水性滤膜不溶于水,水溶液润湿法无法使膜孔被水充填,因此无法测试泡点压力数据。 原理:水侵入法(WIT)通过向疏水性滤膜施加低于其水穿透点压力(WPP)的空气压力,利用水在毛细管作用下优先侵入最大膜孔的现象,通过测量上游空气压力降来评估滤膜完整性的非破坏性测试方法——实测水侵入流量值≤滤器出厂允许最大值,重复测试偏差≤10%,即为合格;若流量异常偏大,说明滤膜存在破损、泄漏。 该方法无需有机溶剂,能有效弥补传统泡点法主观性强、操作繁琐的局限性,且符合GMP及ISO相关标准要求。 操作流程 滤芯润湿与装水 将疏水性滤芯装入滤壳,从上端缓慢加入纯化水,确保水位淹没滤芯 3-5cm。保持 15-30 分钟,让滤芯充分润湿。 连接仪器与设定 关闭上游阀门,将完整性测试仪连接到滤壳上。在仪器上设定好测试压力、稳压时间和测试时间等参数。 启动自动测试 启动仪器,设备会自动进行稳压和加压。在设定的时间内,仪器会自动监测水侵入的数值(或压力降),测试结束后自动打印并显示结果。 排空与干燥 测试完成后,打开滤壳底部的排污阀,将水彻底排空。最后通入洁净的压缩空气,将滤壳和滤芯吹干,即可准备投入使用。 水侵入法检测失败故障排查思路 • 检查检测参数 • 温度在检测过程中稳定(<±1℃):水、环境 • 滤芯干燥,长期使用滤膜可能受潮 • 重新装满水和重新检测滤芯 • 使用前进流方法进行重新检测 • 使用低表面张力的溶液润湿去除污染物后重新检测 泡点法、扩散流法(备选,特殊场景使用) 仅当水侵入法不适用(如滤器特殊材质、高孔径场景)时选用,泡点法实测值≥滤器出厂最低值、保压压力下降≤0.02 bar/min;扩散流法实测值≤允许值,即为合格;操作要点简化如下,核心仍以水侵入法为主: 泡点法:用无水乙醇润湿滤膜,缓慢升压至出现连续气泡,记录泡点值,保压1-2分钟确认稳定; 扩散流法:压力设定为泡点值的80%-90%,测量扩散流值,重复测试确保偏差≤10%。 03、避坑指南:6个高频误区,千万别踩! 1. 误区1:用水做检测介质——错!疏水性滤器不吸水,必须用无水乙醇等兼容介质,且需脱气; 2. 误区2:滤膜未充分润湿——会导致泡点值偏低、扩散流异常,一定要彻底润湿并排出气泡; 3. 误区3:测试仪不校准——每年至少校准1次,校准记录要留存,否则检测数据无效; 4. 误区4:忽略环境控制——温湿度波动过大,会影响压力和介质状态,需实时记录环境参数; 5. 误区5:使用后不验证——按风险等级,使用后需做回顾性或即时验证,不能省略; 6. 误区6:记录补记、涂改——检测记录要实时、准确、完整,严禁补记、涂改,签字确认后不得随意修改。 总结 疏水性滤器完整性检测 首推水侵入法,守住无菌底线 疏水性除菌滤器的完整性检测,核心就两件事:流程规范、数据可追溯,而水侵入法作为首推方法,凭借操作简便、无需有机溶剂、符合合规要求的优势,成为制药、生物制品行业的优选方案。 它不是额外的“负担”,而是规避质量风险、满足GMP/ISO审核的关键环节。掌握水侵入法的操作流程和要点,无论是日常检测,还是应对各类审计,都能从容应对。 你在水侵入法操作过程中,还遇到过哪些问题?欢迎在评论区留言交流,一起避坑、提升实操效率~ 关于康成百澳生物 生命科学领域快速消费品及配套服务的专业供应商,总部位于泰州医药城,上海、广州、南京、成都、苏州、杭州、武汉等地设有分公司及办事处。 产品线涵盖精准医疗、抗体、疫苗、CGT、分子生物学与细胞生物学、常规临床检验、药物筛选、基因组学与蛋白质组学等研究和应用领域,以“技术+产品+服务”的一体化模式服务客户。 部分图片、字体、文字来源于网络 如有侵权请联系删除